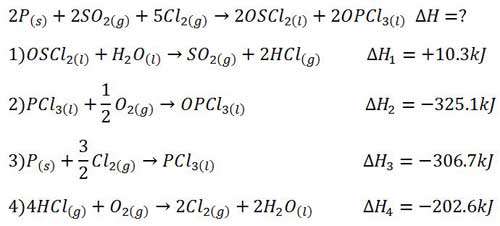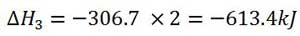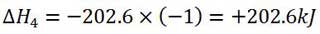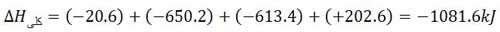شرح درس:
بسیاری از واکنش ها در شرایط سختی انجام می شوند. گاهی یک واکنش شیمیایی ممکن است جزئی از یک فرایند زیست شناختی پیچیده باشد و نتوان آن را به صورت یک واکنش جداگانه در آزمایشگاه انجام داد. به همین دلیل نمی توان گرمای چنین واکنش هایی را از روش مستقیم به دست آورد و باید به دنبال روش های دیگری بود.
به واکنش تولید آمونیاک توجه کنید:

می خواهیم ∆H این واکنش را بدست آوریم. اما این واکنش به همین صورت انجام نمی شود بلکه در دو مرحله روی می دهد و برای محاسبه ∆H آن به اطلاعات دیگری نیز احتیاج داریم. دو واکنش زیر را در نظر بگیرید؛

از جمع این دو واکنش، واکنش تولید آمونیاک به دست می آید. در حقیقت ابتدا هیدرازین (N2H4) تولید شده و سپس آمونیاک به وجود می آید. برای محاسبه آنتالپی واکنش تولید آمونیاک به روش غیر مستقیم می توان از قانون هس استفاده کرد.
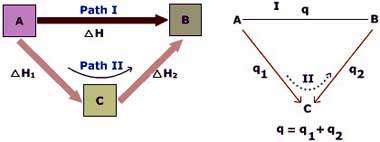
طبق قانون هس اگر یک واکنش، حاصل جمع دو یا چند واکنش دیگر باشد، ∆H واکنش کلی برابر مجموع جمع جبری مقادیر ∆H واکنش های تشکیل دهنده آن است.

همانطور که قبلا گفته شد آنتالپی تابع حالت است و اگر یک واکنش شیمیایی از چند مسیر مختلف انجام شود مقدار تغییر آنتالپی آن در همه مسیرها یکسان بوده و تنها به حالت آغازی و پایانی فرایند بستگی دارد.

بسیاری از واکنش ها در شرایط سختی انجام می شوند. گاهی یک واکنش شیمیایی ممکن است جزئی از یک فرایند زیست شناختی پیچیده باشد و نتوان آن را به صورت یک واکنش جداگانه در آزمایشگاه انجام داد. به همین دلیل نمی توان گرمای چنین واکنش هایی را از روش مستقیم به دست آورد و باید به دنبال روش های دیگری بود.
به واکنش تولید آمونیاک توجه کنید:
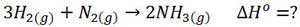
می خواهیم ∆H این واکنش را بدست آوریم. اما این واکنش به همین صورت انجام نمی شود بلکه در دو مرحله روی می دهد و برای محاسبه ∆H آن به اطلاعات دیگری نیز احتیاج داریم. دو واکنش زیر را در نظر بگیرید؛
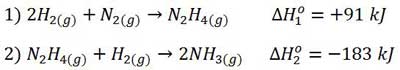
از جمع این دو واکنش، واکنش تولید آمونیاک به دست می آید. در حقیقت ابتدا هیدرازین (N2H4) تولید شده و سپس آمونیاک به وجود می آید. برای محاسبه آنتالپی واکنش تولید آمونیاک به روش غیر مستقیم می توان از قانون هس استفاده کرد.
طبق قانون هس اگر یک واکنش، حاصل جمع دو یا چند واکنش دیگر باشد، ∆H واکنش کلی برابر مجموع جمع جبری مقادیر ∆H واکنش های تشکیل دهنده آن است.
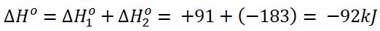
همانطور که قبلا گفته شد آنتالپی تابع حالت است و اگر یک واکنش شیمیایی از چند مسیر مختلف انجام شود مقدار تغییر آنتالپی آن در همه مسیرها یکسان بوده و تنها به حالت آغازی و پایانی فرایند بستگی دارد.